手性固定相系列介绍(一)——多糖类
在手性分析中,使用高效液相色谱方法占80%左右,而在高效液相色谱手性色谱柱的使用中,多糖类手性柱的使用率在70%以上。多糖类手性识别材料还被用于电色谱、超临界色谱、手性高分子膜、薄层色谱,在其他的一些领域如毛细管电泳、毛细管气相色谱、高速逆流色谱、手性传感器等方面也有研究报道。今天小研带大家了解多糖类手性固定相。
多糖类衍生物主要是通过酯化或醚化糖单元上的羟基制备的,酰氯和异氰酸酯是最常用的衍生化试剂。除最常用的纤维素和淀粉外,甲壳素、壳聚糖、半乳糖胺、木聚糖、葡聚糖、凝胶多糖和菊糖也用于多糖类手性固定相的制备。其中,纤维素和淀粉衍生物的手性识别能力通常高于其他多糖类衍生物,在HPLC手性分离中应用最广泛。 多糖类手性固定相是指利用多糖及其衍生物作为手性选择剂,通过涂敷或键合等方式固定在载体表面所形成的。据统计大约有80-90%的化合物,可以通过使用该类手性固定相的色谱柱配合方法开发策略实现拆分。 多糖类手性固定相主要分为纤维素和直链淀粉及其衍生物类。 1)纤维素: 纤维素是D-葡萄糖单元由 β-1,4-糖苷键形成的高度有序、呈螺旋形空穴结构的光学活性天然高分子。由于葡萄糖单元具有手性以及聚合物分子的单手螺旋性质,可以经衍生化用作手性识别材料。对映体分子与纤维素手性空穴的空间匹配程度主要取决于纤维素及其衍生物的构象。多糖衍生物手性固定相的手性识别过程被认为是对映体分子插入多糖衍生物的手性空穴,与手性糖中的极性基团相互作用。因对映体分子与手性空穴的空间匹配程度不同,这种相互作用强度亦有差异,正是这种相互作用强度的差异,使各对映体的保留时间不同。 (多糖类—纤维素) 2)直链淀粉: 直链淀粉与纤维素一样也是一种线型多聚物,是由D-葡萄糖单元由α-1,4-糖苷键连接而成的链状分子,呈右手螺旋结构,每6个葡萄糖单位组成螺旋的1个节距,在螺旋内部只含氢原子,是亲油的,羟基位于螺旋外侧。由于直链淀粉具有确定的分子结构,对应的衍生物具有良好的手性识别能力,所以该类手性识别材料主要以直链淀粉为起始物质进行合成。直链淀粉没有一定的大小,不同来源的直链淀粉分子量差别很大,有些的聚合度DP只有几百,而另外的一些可以是数千。 (多糖类—直链淀粉) 有文献统计在多糖柱中使用频率从高到低的次序为,直链淀粉-三(3,5-二甲基苯基氨基甲酸酯)、纤维素-三(3,5-二甲基苯基氨基甲酸酯)、纤维素-三(4-甲基苯甲酸酯)、纤维素-三(3,5-二氯苯基氨基甲酸酯)、直链淀粉-三((S)-1-苯基乙基氨基甲酸酯)、直链淀粉-三(3,5-二甲基苯基氨基甲酸酯)柱和纤维素-三(3,5-二甲基苯基氨基甲酸酯)柱,是手性高效液相色谱中最广泛使用的商品柱,大约能识别65%以上的手性化合物,成为液相色谱手性柱的首选。 以广州研创EnantioPak® Y3为例,其硅胶表面涂敷有直链淀粉-三(3,5- 二甲基苯基氨基甲酸酯),其特有左手四重螺旋结构,氨基甲酸酯围绕主链形成很多沟槽,所以淀粉型手性色谱柱比纤维素型对于某些样品表现出截然不同的强大分离能力。 硅胶表面涂敷有直链淀粉-三(3,5-二甲基苯基氨基甲酸酯) 一些在纤维素衍生物固定相Y1上不能拆分的样品,在Y3上却能够很好地拆分。特别适用于烃、卤化合物、氰化合物、胺、羧酸、醇类、醚类及其衍生物手性拆分。 Y3目前可进行公斤级生产,性能优异且稳定。禁止使用EA、DCM、DMSO、丙酮等强溶解性溶剂作为流动相或溶剂溶解样品,会对柱子产生不可逆的损害。 Y3比较特殊,是涂覆型手性固定相里唯一可以使用THF作为溶剂溶解样品的色谱柱,对一些常规溶剂溶解性不好的样品有奇效。有不同规格的分析柱,不同内径粗细的半制备柱、制备柱以及保护柱,您可根据实验需要选择合适的规格。 (详情请咨询18922204815) 手性色谱柱分离原理是将具有光学活性的单体固定在硅胶或其他聚合物上制成手性固定相,通过引入手性环境使得对映异构体呈现物理特征的差异,从而达到光学异构体拆分的目的。 目前,手性识别模型多是基于Dalgliesh在1952年提出的“三点相互作用”(Three-point interaction)理论:在一对对映体和手性选择剂之间,为了形成稳定性不同的非对映体分子络合物(Molecule associates)而达到手性分离的目的,至少需要三个同时发生的分子之间的相互作用力起作用。 如下图所示,设对映体的三个原子或基团a、b、c,相应受体的活体作用点为A、B、C,其中一个对映体的a、b、c能与受体的A、B、C很好吻合,至多两个点能吻合,因此两对映体与受体的结合程度就出现差异,相互作用能力不同,表现出不同的生物活性。 对映体与多糖类手性固定相可能存在的相互作用有:①氢键(或 π-π)作用;②π-π作用 ③偶极-偶极相互作用;④ 手性空腔的立体包含作用。⑤过渡金属离子的配位作用等。 纤维素的结构单元中具有多个手性碳,纤维素的苯基氨基甲酸酯衍生物具有左旋 3/2 螺旋结构,苯基氨基甲酸酯基围绕着主链形成许多手性空穴在手性空穴中靠近纤维素主链的外侧是芳基,内侧是手性材料的氨基甲酸酯残基对映体进人手性空穴中进行多次作用,从而达到手性识别。 该类手性固定相的手性识别能力主要来源于样品分子与极性的氨基甲酸酯基基团中的-NH、-C-0的氢键作用,以及与-C=0的偶极-偶极作用,其中对手性识别起主导作用的是氢键作用。 另外,取代基的吸电子性和供电子性对-NH基上氢的活性也有影响。在纤维素的衍生物中大都还引入苯基,这有利于提高手性识别能力。进一步的机理还有待于深入研究。
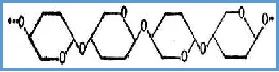




多糖类手性固定相的制备方法主要包括整体成球法、涂敷法和化学键合法。 整体成球法:此法不需要硅胶作载体,而是直接把纤维素衍生物做成凝胶颗粒当作固定相使用。此类固定相的制作方法简单,制备成本低,固定相的柱载量高,但使用寿命相对较短,分析速度较慢。 涂敷法:将多糖衍生物溶于有机溶剂中,然后通过溶剂蒸发或溶剂沉淀法把多糖衍生物涂敷在载体上。此法得到的固定相机械强度和柱效都得到很大改善。然而,由于多糖类衍生物自身的溶解性,流动相溶剂体系的选择受到一定限制。 化学键合法:多糖衍生物通过间隔臂键合在载体上或使衍生物发生交联而固载在载体上。这种方法得到的固定相稳定性好,使用寿命长,且对流动相的选择性较小。
优势: 广泛应用:多糖类手性固定相是运用最普遍的一类固定相,常见于纤维素类手性固定相和直链淀粉类手性固定相。因其稳定性好、应用范围广,可用于HPLC、SFC、SMB等多种色谱分离技术中,对多种手性化合物进行有效拆分。 高效的手性识别能力:天然多糖类分子在手性拆分中并不是很有效,但多糖上的羟基与酯类基团反应后,可制成分离效率高、重现性好、有较强手性识别能力的手性固定相。例如,纤维素-三(3,5-二甲基苯基氨基甲酸酯)和直链淀粉-三(3,5-二甲基苯基氨基甲酸酯)等,对大多数对映体表现出了杰出的识别能力。 多样的合成方法:多糖类手性固定相的合成方法多样,如双官能团法、端基还原法、自由基共聚法、光化学法、施陶丁格反应和分子间共聚法等。其中,施陶丁格反应和分子间共聚法制备的手性固定相手性识别能力、稳定性均较高,过程相对简单,重现性好。 良好的稳定性:键合型多糖类手性固定相克服了涂敷型手性固定相的缺点,扩大了流动相的选择范围,提高了手性固定相的稳定性。对于部分失效的固定相,可用一些修复方法再生,恢复手性识别能力。 局限: 流动相选择限制:涂敷型多糖类手性固定相在选择有机溶剂作为流动相时存在许多局限性,可能会破坏手性固定相的结构,影响分离效果。 合成复杂性:虽然多糖类手性固定相的合成方法多样,但某些方法(如端基还原法)过程复杂,且只适用于特定类型的多糖衍生物。 手性拆分能力的差异:多糖类手性固定相的手性拆分能力可能受到取代基种类、位置和数量的影响。例如,某些取代基可能使手性固定相对某些类型的手性化合物具有更高的识别能力,而对其他类型的化合物则识别能力较低。 参考文献: 1. 手性识别材料(第二版),袁黎明 编著 2. 手性药物分析,尤启东、林国强 编著 下期预告:具有空腔结构的环糊精类固定相介绍


 地址:广州市黄埔区揽月路3号国际企业孵化器F座310
地址:广州市黄埔区揽月路3号国际企业孵化器F座310 电话:18922204815
电话:18922204815  传真:020-84418344
传真:020-84418344 邮箱:mzzhang@chiral-se.com
邮箱:mzzhang@chiral-se.com

